Нетипичные значения коэффициентов Бренстеда
В состав кислоты Бренстеда входит протон и сопряженное основание -- его переносчик. В промежуточном состоянии переноса протона, последний находится между двумя основаниями. Исходное основание, отдающее протон и новое, которое протон принимает. Протон полностью будет принадлежать новому основанию в продукте реакции.
Насколько более полно протон в переходном состоянии переносится к продукту реакции, настолько больше влияние структурных изменений на константу скорости должно соответствовать влиянию и на константу равновесия.
Структурные изменения появляются при введении в молекулу кислоты или основания заместителей.
Чем ближе коэффициент $\beta $ будет к единице, тем больше степень переноса протона к основанию. Соответственно, чем ниже $\beta $, тем меньше степень образования связи.
Изменения значений коэффициента $\alpha $ находится в зависимости от значительного или незначительного переноса протона от кислоты в промежуточном состоянии.
Случаи аномального проявления значений $\alpha $ и $\beta $:
Коэффициент $\alpha
Пример 1Для нитроалканов $\alpha =-0,48$
\[R_2CHNO_2{{\stackrel{{OH}^-}{\longrightarrow}}}{(R_2CNO_2)}^-+H_2O,\]при $R=H, CH_3$
Коэффициент $\alpha > 1.$
Пример 2Реакции серии $1$-арил-$2$-нитропропанов, перенос протона к группе $OH^-$ в водном метаноле при $\alpha =1,68.$
\[ArCH_2CH(CH_3)\ NO_2{{\stackrel{{OH}^-}{\longrightarrow}ArCH_2C\left(CH_3\right)NO_2+H_2O.}}\]Для обратной реакции $\beta=-0,68.$ Нетипичное поведение 1-арил-2-нитропропанов при депротонировании заключается в том, что энергия переходного состояния при изменении исходного соединения, меняется сильнее, чем энергия продукта реакции.
Зависимость кривизны графика Бренстеда от силы кислоты
В случае, когда с одним основанием реагирует ряд кислот разной силы, то параметр $\alpha $ должен меняться в пределе от $0$ до $1$.
\[AH + B ↔ [A\dots H\dots B] ↔ BH^+ + A^-,\]где $[A\dots H\dots B]$ отображает переходное состояние.
Если кислота очень слабая, то переходного состояния можно достичь при практически полном переносе протона, то есть $\alpha >1$. При этом сопряженное основание намного сильнее принимающего основания.
Если кислота слабая, то есть сопряженное основание значительно слабее принимающего основания, $\alpha >0$, то переходное состояние достигается рано
Если с одним и тем же основанием $B$ будет реагировать серия кислот $AH$, то сумма коэффициентов для прямой и обратной реакции будет равна единице.
\[AH + B {{\stackrel{K_{AH}}{\longrightarrow}}} BH^+ + A^-\]\[BH^+ + A-{{\stackrel{K_{А^-}}{\longrightarrow}}} B + HA\]\[lgK=lgK_{AH}-lgK_{А^-}=-pK_a\left(AH\right)+pK_a\left(BH^+\right),\]где $K=K_{AH}/K_A$ - константа равновесия $AH+B → BH^+ + A^-.$
Тогда $lgK_{А^-}=\left(1-\alpha \right)pK_a\left(AH\right)+lgK_a\left(BH^+\right)+const.$
Коэффициент $\beta $ для обратной реакции будет равен $1-\alpha $.
Таким образом, при значительных изменениях $HA$ величина коэффициента $\alpha $ будет изменяться. В таких случаях графики Бренстеда уже не будут линейными.
Взаимосвязь между константами скоростей и равновесия и кривизной графика Бренстеда
Рассмотрим реакции кетонов, эфиров и кето-эфиров с основаниями. Корреляция между величинами $lg(k/p_1g_1)$ и $lg(q_1p_2K/q_2p_1)$ представлена на рис. 1. $p_1$, $g_1$, $p_2$, $q_2$- статистические параметры, относящиеся соответственно к кетону и основанию. $K$-- константа равновесия реакции. Она равна отношению констант диссоциации кетона и кислоты, сопряженной основанию.
Точки, соответствующие значениям $K$, подтверждают внутреннюю согласованность соотношения, представляемого кривой графика, но при этом не служат для нее независимой основой.
Представленный график свидетельствует о корреляции среди однотипных соединений, состоящих из набора кетонов или оснований.
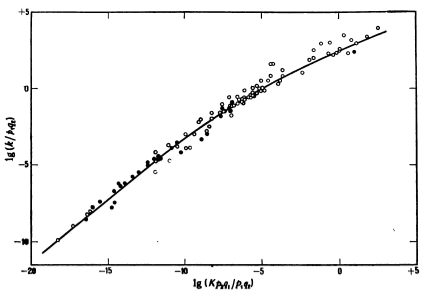
Рисунок 1. Взаимосвязь между константами скоростей и равновесия для реакций кетонов, эфиров и кето-эфиров с основаниями
Данный график заметно искривлен. Величина наклона изменяется в два раза на протяжении всего интервала значений констант равновесий.
Кривизна графика является результатом того, что для катализируемых основаниями реакций кетонов показатель экспоненты уменьшается по мере повышения реакционной способности субстрата.
Анализ таких корреляций широко используют в настоящее время для выяснения влияния заместителей или природы растворителя на термодинамику и кинетику органических реакций.
Соотношение Бренстеда требует особой интерпретации, базирующейся на молекулярных представлениях, применительно к реакциям переноса протона.
Хориути и Поляни, Белл в рамках ковалентной и ионной моделей, предложили обоснование соотношения Бренстеда используя кривые потенциальной энергии.
Реакция переноса протона является специальным случаем процессов типа $XZ + Y → X + ZY.$ Изменение энергии в результате этой реакции можно изобразить при помощи энергетической диаграммы (Рис. 2).
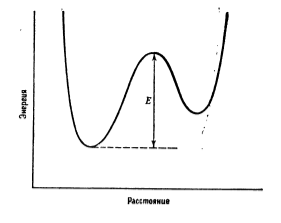
Рисунок 2. Энергетический профиль для реакции переноса протона
В данном случае энергетический профиль представлен двумерной диаграммой, которая является сечением указанной энергетической поверхности. Рассматриваются конфигурации, которые отвечают только линейному расположению частиц $X, Z, Y$ и наиболее вероятный путь реакции описывается линией, ведущей из начального состояния в конечное вдоль контура с наименьшей энергией.
Для абсолютно точного описания энергетического профиля, полная энергетическая поверхность должна быть четырехмерной.

















